Categorieën
-
FSC Koltsova - "Vita 12"
-
FSC Koltsova - "Blue-basic serie"
-
FSC Koltsova - "Plaatsen van macht"
-
FSC Koltsova - "Cosmo-energetica"
-
FSC Koltsova - "Gouden Serie"
-
FSC Koltsova - "Collector-serie"
-
FSC Koltsova - "Exclusieve serie"
-
FSC Koltsova - "Elite-serie"
-
FSC Koltsova - "Myriaden"
-
FSC Koltsova - "Arcanum-serie"
-
FSC Koltsova - "Bescherming voor de telefoon"
-
FSC Koltsova - "Armbanden"
-
Collageen
-
OXYchlorofyllijn
-
Biologisch actieve voedingssupplementen








 Een vreemde formulering van de vraag over wat de meest voorkomende en meest wijdverbreide stof ter wereld lijkt te zijn, komt echter voort uit één boek over het water naar een andere met hetzelfde doel: de lezer intrigeren. Het lijkt je alsof je iets over water weet, maar in feite zit er iets mysterieus en onkenbaars in, waar je je niet eens van bewust bent. Deze achtergrond van deze vraag werd steevast gevoeld en vervolgens versterkt door een opsomming van de vreemde eigenschappen van water die de vorm van de vraag rechtvaardigden.
Een vreemde formulering van de vraag over wat de meest voorkomende en meest wijdverbreide stof ter wereld lijkt te zijn, komt echter voort uit één boek over het water naar een andere met hetzelfde doel: de lezer intrigeren. Het lijkt je alsof je iets over water weet, maar in feite zit er iets mysterieus en onkenbaars in, waar je je niet eens van bewust bent. Deze achtergrond van deze vraag werd steevast gevoeld en vervolgens versterkt door een opsomming van de vreemde eigenschappen van water die de vorm van de vraag rechtvaardigden.  Om het primaire beeld te verkrijgen hebben veel wetenschappers besteed Er is de afgelopen eeuw veel aandacht besteed aan de structurele toestand van het water. Maar volgens de meeste experts was het tot voor kort niet mogelijk om een bevredigend beeld te krijgen bij het maken van structurele modellen van water. Deze omstandigheid werd enigszins duidelijker toen de redenen voor dergelijke mislukte pogingen op het gebied van wateronderzoek werden geïdentificeerd. Als water eerder, met de gebruikelijke thermodynamische benadering, had moeten worden beschouwd als een statistisch systeem van chaotisch op elkaar inwerkende moleculen, hebben recente studies de mogelijkheid aangetoond van een kwalitatief andere benadering die rekening houdt met de initiële structurele kenmerken van het watermolecuul en de gerichte aard van het proces van vorming van waterstofbruggen (Fig. 1), dat wil zeggen een bepaalde volgorde in de volgorde van interactie van centra voor de vorming van waterstofbruggen in water.
Om het primaire beeld te verkrijgen hebben veel wetenschappers besteed Er is de afgelopen eeuw veel aandacht besteed aan de structurele toestand van het water. Maar volgens de meeste experts was het tot voor kort niet mogelijk om een bevredigend beeld te krijgen bij het maken van structurele modellen van water. Deze omstandigheid werd enigszins duidelijker toen de redenen voor dergelijke mislukte pogingen op het gebied van wateronderzoek werden geïdentificeerd. Als water eerder, met de gebruikelijke thermodynamische benadering, had moeten worden beschouwd als een statistisch systeem van chaotisch op elkaar inwerkende moleculen, hebben recente studies de mogelijkheid aangetoond van een kwalitatief andere benadering die rekening houdt met de initiële structurele kenmerken van het watermolecuul en de gerichte aard van het proces van vorming van waterstofbruggen (Fig. 1), dat wil zeggen een bepaalde volgorde in de volgorde van interactie van centra voor de vorming van waterstofbruggen in water. 
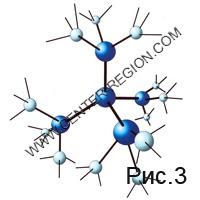
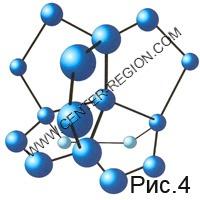
 Natuurlijk kan de veronderstelde symmetrische omgeving van één watermolecuul met vier extra (Fig. 2) voor een extreem korte tijd bestaan. Maar de centra voor de vorming van waterstofbruggen in elk van de vier externe moleculen, waarvan er voor elk drie over zijn, zijn qua waarschijnlijkheid van interactie niet slechter dan de reeds gereageerde centra, en er kunnen op een gegeven moment ook watermoleculen mee verbonden worden (Fig. 3). Een dergelijke zeventien-moleculaire formatie kan natuurlijk alleen hypothetisch worden voorgesteld vanwege het bestaan ervan op de korte termijn, maar de geometrie van de onderlinge rangschikking van waterstofbruggen onder een hoek dichtbij de tetraëder en de hoek van de vijfhoek geeft onverwachts een kans om de levensduur van zijn bestaan te verlengen als gevolg van de vorming van zes vijfledige cycli tegelijk (Fig. 4). Volgens chemisch-kinetische concepten verschijnt er in dit geval als het ware een smalle concentratiestroom van de stroom van medewerkers naar een bestaan op langere termijn. De toename van de levensduur vindt plaats als gevolg van de verdieping van de potentiële energiebron waarin alle 17 moleculen zich bevinden, onmiddellijk met een hoeveelheid gelijk aan zes energieën voor de vorming van waterstofbruggen. Maar het belangrijkste is niet eens dit, maar de opkomende geometrie van het neoplasma. Dezelfde opstelling van zes centra voor de vorming van waterstofbruggen verschijnt in één vlak, die, onder de voorwaarde van complementariteit, op het punt staan te ‘instorten’ met een vergelijkbare formatie als gevolg van de miljoenste interactieconstante.
Natuurlijk kan de veronderstelde symmetrische omgeving van één watermolecuul met vier extra (Fig. 2) voor een extreem korte tijd bestaan. Maar de centra voor de vorming van waterstofbruggen in elk van de vier externe moleculen, waarvan er voor elk drie over zijn, zijn qua waarschijnlijkheid van interactie niet slechter dan de reeds gereageerde centra, en er kunnen op een gegeven moment ook watermoleculen mee verbonden worden (Fig. 3). Een dergelijke zeventien-moleculaire formatie kan natuurlijk alleen hypothetisch worden voorgesteld vanwege het bestaan ervan op de korte termijn, maar de geometrie van de onderlinge rangschikking van waterstofbruggen onder een hoek dichtbij de tetraëder en de hoek van de vijfhoek geeft onverwachts een kans om de levensduur van zijn bestaan te verlengen als gevolg van de vorming van zes vijfledige cycli tegelijk (Fig. 4). Volgens chemisch-kinetische concepten verschijnt er in dit geval als het ware een smalle concentratiestroom van de stroom van medewerkers naar een bestaan op langere termijn. De toename van de levensduur vindt plaats als gevolg van de verdieping van de potentiële energiebron waarin alle 17 moleculen zich bevinden, onmiddellijk met een hoeveelheid gelijk aan zes energieën voor de vorming van waterstofbruggen. Maar het belangrijkste is niet eens dit, maar de opkomende geometrie van het neoplasma. Dezelfde opstelling van zes centra voor de vorming van waterstofbruggen verschijnt in één vlak, die, onder de voorwaarde van complementariteit, op het punt staan te ‘instorten’ met een vergelijkbare formatie als gevolg van de miljoenste interactieconstante. 
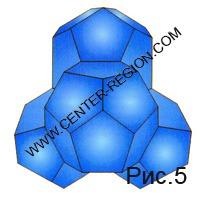
 Een "stroompje" van de stroom van medewerkers naar een bestaan op langere termijn in elk van de zes potentiële energiegaten van het 17 moleculaire skelet “vond” de volgende verdieping van de potentiële put, ook gelijk aan zes waterstofbrugenergieën. Als gevolg hiervan verschijnt een prachtige geometrische figuur (Fig. 5) - een dodecaëdrische tetraëder [7,8], die bij verdere constructie als het ware een soort "kwantum" wordt - een soort handige baksteen voor constructie.
Een "stroompje" van de stroom van medewerkers naar een bestaan op langere termijn in elk van de zes potentiële energiegaten van het 17 moleculaire skelet “vond” de volgende verdieping van de potentiële put, ook gelijk aan zes waterstofbrugenergieën. Als gevolg hiervan verschijnt een prachtige geometrische figuur (Fig. 5) - een dodecaëdrische tetraëder [7,8], die bij verdere constructie als het ware een soort "kwantum" wordt - een soort handige baksteen voor constructie. 
 Het zal waarschijnlijk vreemd lijken dat zo'n krachtige toename van het aantal watermoleculen en vervolgens het aantal “quanta” bij medewerkers kan plotseling een einde komen. Het antwoord bleek uiterst eenvoudig. De waarschijnlijkheid van complementaire interactie tegelijk met zes, toen achttien en nu vierentwintig centra voor de vorming van waterstofbruggen nam snel af als gevolg van een sterke toename van het aantal combinaties dat moet worden uitgezocht om een complementaire combinatie te ‘struikelen’. Daarom werd een dergelijke krachtige toename van de bindingsconstante in deze centra gecompenseerd door een even krachtige afname van de waarschijnlijkheid van complementaire interactie. Op het niveau van vierentwintig centra stopte de waterstofbinding.
Het zal waarschijnlijk vreemd lijken dat zo'n krachtige toename van het aantal watermoleculen en vervolgens het aantal “quanta” bij medewerkers kan plotseling een einde komen. Het antwoord bleek uiterst eenvoudig. De waarschijnlijkheid van complementaire interactie tegelijk met zes, toen achttien en nu vierentwintig centra voor de vorming van waterstofbruggen nam snel af als gevolg van een sterke toename van het aantal combinaties dat moet worden uitgezocht om een complementaire combinatie te ‘struikelen’. Daarom werd een dergelijke krachtige toename van de bindingsconstante in deze centra gecompenseerd door een even krachtige afname van de waarschijnlijkheid van complementaire interactie. Op het niveau van vierentwintig centra stopte de waterstofbinding.  Een stabiel structureel element heeft op zijn zijden gedeeltelijk geladen zuurstof- en waterstofatomen, en wanneer het roteert rond het zwaartepunt, bevinden negatief geladen zuurstofatomen zich 1,09 angstrom dichter bij het centrum dan positief geladen waterstofatomen (Fig. 10). Maar dit betekent dat het gebied van de cirkel dat wordt geschetst door de beweging van positieve ladingen kleiner is dan het gebied van de cirkel dat wordt geschetst door de beweging van negatieve ladingen. Hun verschil bepaalt het niet-gecompenseerde magnetische moment van het element, waardoor het probleem van het verkeerd begrijpen van het effect van een magnetisch veld op water onmiddellijk wordt geëlimineerd.
Een stabiel structureel element heeft op zijn zijden gedeeltelijk geladen zuurstof- en waterstofatomen, en wanneer het roteert rond het zwaartepunt, bevinden negatief geladen zuurstofatomen zich 1,09 angstrom dichter bij het centrum dan positief geladen waterstofatomen (Fig. 10). Maar dit betekent dat het gebied van de cirkel dat wordt geschetst door de beweging van positieve ladingen kleiner is dan het gebied van de cirkel dat wordt geschetst door de beweging van negatieve ladingen. Hun verschil bepaalt het niet-gecompenseerde magnetische moment van het element, waardoor het probleem van het verkeerd begrijpen van het effect van een magnetisch veld op water onmiddellijk wordt geëlimineerd.  De verscheidenheid aan ladingspatronen op de vlakken van structurele elementen stelt ons in staat de aard van hun daaropvolgende interacties te suggereren. In werkelijkheid is elk element omgeven door andere structurele elementen met een wederzijds complementaire ladingsverdeling (Fig. 11). Het is duidelijk dat de vlakken met niet-gecompenseerde ladingen met de eerste ladingen zullen interageren, aangezien uit de 24 centra voor de vorming van waterstofbruggen er zullen niet altijd precies 12 zuurstofatomen zijn en dienovereenkomstig 12 waterstofatomen op elk vlak. Dan moeten we de interactie verwachten van de zogenaamde matrix-gepolariseerde vlakken, wanneer een algemeen ladingsneutraal vlak ruimtelijk gescheiden groepen ladingen met verschillende tekens heeft van dergelijke geladen plaatsen op de vlakken is het mogelijk dat er ladingen verschijnen op de resterende laterale centra van de vorming van waterstofbruggen die niet betrokken zijn bij de vorming van het structurele element [11]. Het bleek interessant om de berekende waarden van het volume van dergelijke verdeelstukken te vergelijken met de experimenteel bepaalde afmetingen van sommige geïsoleerde sets die enigszins te onderscheiden zijn op een contrastfasemicroscoop, zeer vergelijkbaar met cellen.
De verscheidenheid aan ladingspatronen op de vlakken van structurele elementen stelt ons in staat de aard van hun daaropvolgende interacties te suggereren. In werkelijkheid is elk element omgeven door andere structurele elementen met een wederzijds complementaire ladingsverdeling (Fig. 11). Het is duidelijk dat de vlakken met niet-gecompenseerde ladingen met de eerste ladingen zullen interageren, aangezien uit de 24 centra voor de vorming van waterstofbruggen er zullen niet altijd precies 12 zuurstofatomen zijn en dienovereenkomstig 12 waterstofatomen op elk vlak. Dan moeten we de interactie verwachten van de zogenaamde matrix-gepolariseerde vlakken, wanneer een algemeen ladingsneutraal vlak ruimtelijk gescheiden groepen ladingen met verschillende tekens heeft van dergelijke geladen plaatsen op de vlakken is het mogelijk dat er ladingen verschijnen op de resterende laterale centra van de vorming van waterstofbruggen die niet betrokken zijn bij de vorming van het structurele element [11]. Het bleek interessant om de berekende waarden van het volume van dergelijke verdeelstukken te vergelijken met de experimenteel bepaalde afmetingen van sommige geïsoleerde sets die enigszins te onderscheiden zijn op een contrastfasemicroscoop, zeer vergelijkbaar met cellen.