Catégories
-
FSC Koltsova - "Vita 12"
-
FSC Koltsova - "Série Blue-basic"
-
FSC Koltsova - "Lieux de pouvoir"
-
FSC Koltsova - "Cosmoénergétique"
-
FSC Koltsova - "Série d'Or"
-
FSC Koltsova - "Série Collector"
-
FSC Koltsova - "Série exclusive"
-
FSC Koltsova - "Série Élite"
-
FSC Koltsova - "Myriades"
-
FSC Koltsova - "Série Arcane"
-
FSC Koltsova - "Protection pour le téléphone"
-
FSC Koltsova - "Bracelets"
-
Collagène
-
Lignée OXYchlorophylle
-
Compléments alimentaires bioactifs








 Une étrange formulation de la question sur ce qui semble être la substance la plus courante et la plus répandue dans le monde migre cependant d'un livre à travers l'eau à une autre dans le même but : intriguer le lecteur. Il vous semble que vous savez quelque chose sur l'eau, mais en fait il y a quelque chose de mystérieux et d'inconnaissable dont vous n'avez même pas conscience. Cet arrière-plan de cette question était invariablement ressenti, puis renforcé par une liste des propriétés étranges de l'eau qui justifiaient la forme de la question.
Une étrange formulation de la question sur ce qui semble être la substance la plus courante et la plus répandue dans le monde migre cependant d'un livre à travers l'eau à une autre dans le même but : intriguer le lecteur. Il vous semble que vous savez quelque chose sur l'eau, mais en fait il y a quelque chose de mystérieux et d'inconnaissable dont vous n'avez même pas conscience. Cet arrière-plan de cette question était invariablement ressenti, puis renforcé par une liste des propriétés étranges de l'eau qui justifiaient la forme de la question.  Pour obtenir l'image principale De nombreux scientifiques ont consacré beaucoup d'efforts à l'état structurel de l'eau au cours du siècle dernier. Mais, selon la plupart des experts, jusqu'à récemment, il n'était pas possible d'obtenir une image satisfaisante lors de la création de modèles structurels de l'eau. Cette situation est devenue un peu plus claire lorsque les raisons de ces tentatives infructueuses de recherche sur l'eau ont été identifiées. Si auparavant, avec l'approche thermodynamique habituelle, l'eau aurait dû être considérée comme un système statistique de molécules en interaction chaotique, des études récentes ont montré la possibilité d'une approche qualitativement différente qui prend en compte les caractéristiques structurelles initiales de la molécule d'eau et la nature dirigée du processus de formation des liaisons hydrogène (Fig. 1), c'est-à-dire un certain ordre dans la séquence d'interaction des centres pour la formation des liaisons hydrogène dans l'eau.
Pour obtenir l'image principale De nombreux scientifiques ont consacré beaucoup d'efforts à l'état structurel de l'eau au cours du siècle dernier. Mais, selon la plupart des experts, jusqu'à récemment, il n'était pas possible d'obtenir une image satisfaisante lors de la création de modèles structurels de l'eau. Cette situation est devenue un peu plus claire lorsque les raisons de ces tentatives infructueuses de recherche sur l'eau ont été identifiées. Si auparavant, avec l'approche thermodynamique habituelle, l'eau aurait dû être considérée comme un système statistique de molécules en interaction chaotique, des études récentes ont montré la possibilité d'une approche qualitativement différente qui prend en compte les caractéristiques structurelles initiales de la molécule d'eau et la nature dirigée du processus de formation des liaisons hydrogène (Fig. 1), c'est-à-dire un certain ordre dans la séquence d'interaction des centres pour la formation des liaisons hydrogène dans l'eau. 
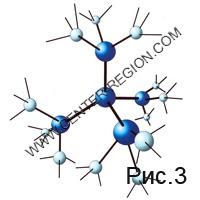
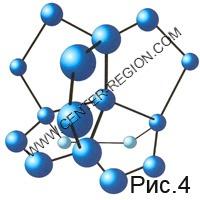
 Bien sûr, l'environnement symétrique supposé d'une molécule d'eau sur quatre autres (Fig. 2) peut exister pendant une période extrêmement courte. Mais les centres de formation de liaisons hydrogène dans chacune des quatre molécules externes, qui en restent trois pour chacune, ne sont pas pires en termes de probabilité d'interaction que les centres déjà réagis, et des molécules d'eau peuvent également y être connectées à un moment donné (Fig. 3). Une telle formation de dix-sept molécules, bien sûr, ne peut être imaginée qu'hypothétiquement en raison de son existence à court terme, mais la géométrie de l'arrangement mutuel des liaisons hydrogène à un angle proche du tétraédrique et de l'angle du pentagone donne de manière inattendue une chance d'augmenter la durée de vie de son existence en raison de la formation de six cycles à cinq chaînons à la fois (Fig. 4). Selon les concepts chimico-cinétiques, dans ce cas, un « flux » de concentration étroite apparaît, pour ainsi dire, du flux d'associés vers une existence à plus long terme. L'augmentation de la durée de vie est due à l'approfondissement du puits d'énergie potentielle dans lequel se trouvent les 17 molécules, d'un montant immédiatement égal à six énergies de formation de liaisons hydrogène. Mais l’essentiel n’est même pas cela, mais la géométrie émergente du néoplasme. Le même agencement de six centres de formation de liaisons hydrogène apparaît dans un plan, qui, dans des conditions de complémentarité, sont prêts à « s'effondrer » avec une formation similaire en raison de la millionième constante d'interaction.
Bien sûr, l'environnement symétrique supposé d'une molécule d'eau sur quatre autres (Fig. 2) peut exister pendant une période extrêmement courte. Mais les centres de formation de liaisons hydrogène dans chacune des quatre molécules externes, qui en restent trois pour chacune, ne sont pas pires en termes de probabilité d'interaction que les centres déjà réagis, et des molécules d'eau peuvent également y être connectées à un moment donné (Fig. 3). Une telle formation de dix-sept molécules, bien sûr, ne peut être imaginée qu'hypothétiquement en raison de son existence à court terme, mais la géométrie de l'arrangement mutuel des liaisons hydrogène à un angle proche du tétraédrique et de l'angle du pentagone donne de manière inattendue une chance d'augmenter la durée de vie de son existence en raison de la formation de six cycles à cinq chaînons à la fois (Fig. 4). Selon les concepts chimico-cinétiques, dans ce cas, un « flux » de concentration étroite apparaît, pour ainsi dire, du flux d'associés vers une existence à plus long terme. L'augmentation de la durée de vie est due à l'approfondissement du puits d'énergie potentielle dans lequel se trouvent les 17 molécules, d'un montant immédiatement égal à six énergies de formation de liaisons hydrogène. Mais l’essentiel n’est même pas cela, mais la géométrie émergente du néoplasme. Le même agencement de six centres de formation de liaisons hydrogène apparaît dans un plan, qui, dans des conditions de complémentarité, sont prêts à « s'effondrer » avec une formation similaire en raison de la millionième constante d'interaction. 
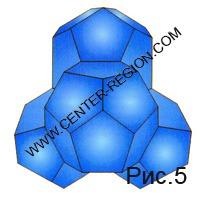
 Un "filet" du flux d'associés vers une existence à plus long terme dans chacun des six trous d'énergie potentielle des 17 squelettes moléculaires a « trouvé » le prochain approfondissement de le potentiel bien, également égal à six énergies de liaison hydrogène. En conséquence, une belle figure géométrique apparaît (Fig. 5) - un tétraèdre dodécaédrique [7,8], qui, pour ainsi dire, devient une sorte de « quantum » dans la construction ultérieure - une sorte de brique pratique pour la construction.
Un "filet" du flux d'associés vers une existence à plus long terme dans chacun des six trous d'énergie potentielle des 17 squelettes moléculaires a « trouvé » le prochain approfondissement de le potentiel bien, également égal à six énergies de liaison hydrogène. En conséquence, une belle figure géométrique apparaît (Fig. 5) - un tétraèdre dodécaédrique [7,8], qui, pour ainsi dire, devient une sorte de « quantum » dans la construction ultérieure - une sorte de brique pratique pour la construction. 
 Il semblera probablement étrange qu'une augmentation aussi puissante du nombre de molécules d'eau, puis du nombre de Les « quanta » chez les associés peuvent soudainement prendre fin. La réponse s’est avérée extrêmement simple. La probabilité d'interaction complémentaire avec six, puis dix-huit et maintenant vingt-quatre centres de formation de liaisons hydrogène a rapidement diminué en raison d'une forte augmentation du nombre de combinaisons qu'il faut trier pour « tomber sur » une combinaison complémentaire. Par conséquent, une augmentation aussi puissante de la constante de liaison au niveau de ces centres a été compensée par une diminution tout aussi puissante de la probabilité d’interaction complémentaire. Au niveau de vingt-quatre centres, les liaisons hydrogène ont cessé.
Il semblera probablement étrange qu'une augmentation aussi puissante du nombre de molécules d'eau, puis du nombre de Les « quanta » chez les associés peuvent soudainement prendre fin. La réponse s’est avérée extrêmement simple. La probabilité d'interaction complémentaire avec six, puis dix-huit et maintenant vingt-quatre centres de formation de liaisons hydrogène a rapidement diminué en raison d'une forte augmentation du nombre de combinaisons qu'il faut trier pour « tomber sur » une combinaison complémentaire. Par conséquent, une augmentation aussi puissante de la constante de liaison au niveau de ces centres a été compensée par une diminution tout aussi puissante de la probabilité d’interaction complémentaire. Au niveau de vingt-quatre centres, les liaisons hydrogène ont cessé.  Un élément structurel stable a sur ses faces des atomes d'oxygène et d'hydrogène partiellement chargés, et lorsqu'il tourne autour du centre de gravité, les oxygènes chargés négativement sont 1,09 angströms plus proches du centre que les hydrogènes chargés positivement (Fig. 10). Mais cela signifie que l'aire du cercle délimitée par le mouvement des charges positives est inférieure à l'aire du cercle délimitée par le mouvement des charges négatives. Leur différence détermine le moment magnétique non compensé de l'élément, ce qui élimine immédiatement le problème d'une mauvaise compréhension de l'effet d'un champ magnétique sur l'eau.
Un élément structurel stable a sur ses faces des atomes d'oxygène et d'hydrogène partiellement chargés, et lorsqu'il tourne autour du centre de gravité, les oxygènes chargés négativement sont 1,09 angströms plus proches du centre que les hydrogènes chargés positivement (Fig. 10). Mais cela signifie que l'aire du cercle délimitée par le mouvement des charges positives est inférieure à l'aire du cercle délimitée par le mouvement des charges négatives. Leur différence détermine le moment magnétique non compensé de l'élément, ce qui élimine immédiatement le problème d'une mauvaise compréhension de l'effet d'un champ magnétique sur l'eau.  La variété des modèles de charges sur les faces des éléments structurels nous permet de suggérer la nature de leurs interactions ultérieures. En réalité, chaque élément est entouré d'autres éléments structurels avec une distribution de charges mutuellement complémentaire (Fig. 11). Il est clair que les faces avec des charges non compensées interagiront en premier, puisque sur 24 centres de formation d'hydrogène liaisons il n'y aura pas toujours exactement 12 atomes d'oxygène et, par conséquent, 12 atomes d'hydrogène sur chaque face. Ensuite, nous devrions nous attendre à l'interaction des faces dites polarisées par la matrice, lorsqu'une face généralement à charge neutre a des groupes de charges de signes différents spatialement séparés. compensation complète de ces endroits chargés sur les faces, il est possible que des charges apparaissent sur les centres latéraux résiduels de formation de liaisons hydrogène qui ne sont pas impliquées dans la formation de l'élément structurel [11]. Il s'est avéré intéressant de comparer les valeurs calculées du volume de tels collecteurs et les tailles déterminées expérimentalement de certains ensembles isolés qui se distinguent quelque peu au microscope à phase de contraste, très similaire aux cellules. La taille d'un demi-micron observée des cellules coïncide assez précisément avec la taille du volume occupé par le nombre de cellules. éléments structurels de tous types, on pourrait supposer que, malgré le caractère labile et stable des formations ultérieures, un certain déterminisme de leur construction doit encore être observé. Trouver des preuves expérimentales de l'existence de différents niveaux structurels de la cellule dans ce cas est beaucoup plus difficile. Par conséquent, l'idée de la structure cellulaire proposée ci-dessous a été obtenue, tout d'abord, en calculant avec précision toutes les combinaisons nécessaires pour compenser d'abord les faces chargées puis les faces polarisées par matrice. La confirmation expérimentale obtenue à l'issue de nos études du modèle cellulaire issu des calculs et la coïncidence étonnamment précise (jusqu'à 0,2%) du nombre d'éléments structurels calculés et réellement impliqués dans la formation de la cellule nous permettent d'offrir une image complète de l'état structurel de la cellule.
La variété des modèles de charges sur les faces des éléments structurels nous permet de suggérer la nature de leurs interactions ultérieures. En réalité, chaque élément est entouré d'autres éléments structurels avec une distribution de charges mutuellement complémentaire (Fig. 11). Il est clair que les faces avec des charges non compensées interagiront en premier, puisque sur 24 centres de formation d'hydrogène liaisons il n'y aura pas toujours exactement 12 atomes d'oxygène et, par conséquent, 12 atomes d'hydrogène sur chaque face. Ensuite, nous devrions nous attendre à l'interaction des faces dites polarisées par la matrice, lorsqu'une face généralement à charge neutre a des groupes de charges de signes différents spatialement séparés. compensation complète de ces endroits chargés sur les faces, il est possible que des charges apparaissent sur les centres latéraux résiduels de formation de liaisons hydrogène qui ne sont pas impliquées dans la formation de l'élément structurel [11]. Il s'est avéré intéressant de comparer les valeurs calculées du volume de tels collecteurs et les tailles déterminées expérimentalement de certains ensembles isolés qui se distinguent quelque peu au microscope à phase de contraste, très similaire aux cellules. La taille d'un demi-micron observée des cellules coïncide assez précisément avec la taille du volume occupé par le nombre de cellules. éléments structurels de tous types, on pourrait supposer que, malgré le caractère labile et stable des formations ultérieures, un certain déterminisme de leur construction doit encore être observé. Trouver des preuves expérimentales de l'existence de différents niveaux structurels de la cellule dans ce cas est beaucoup plus difficile. Par conséquent, l'idée de la structure cellulaire proposée ci-dessous a été obtenue, tout d'abord, en calculant avec précision toutes les combinaisons nécessaires pour compenser d'abord les faces chargées puis les faces polarisées par matrice. La confirmation expérimentale obtenue à l'issue de nos études du modèle cellulaire issu des calculs et la coïncidence étonnamment précise (jusqu'à 0,2%) du nombre d'éléments structurels calculés et réellement impliqués dans la formation de la cellule nous permettent d'offrir une image complète de l'état structurel de la cellule.